Успехи фармацевтической промышленности позволяют России претендовать на серьезные позиции на мировом рынке инновационных лекарственных препаратов. Но прежде государство должно разработать эффективные меры поддержки компаний, которые инвестируют в разработку новых молекул, и определить сами критерии инновационности.
Текст: Ирина ЖАВОРОНКОВА
Здоровье на экспорт
В 2018 году российский фармрынок вырос более чем на 10%. При этом список жизненно необходимых и важнейших лекарственных препаратов (ЖНВЛП) увеличился на 60 позиций, а доля российских производителей в нем достигла рекордных 84%. В 2019 году к перечню должны добавиться еще 38 препаратов.
Стоящая перед государством задача, однако, не ограничивается импортозамещением, а куда более амбициозна. Россия рассчитывает на кратный рост экспорта фармпродукции. В первую очередь — за счет «развития сегмента инновационных лекарственных препаратов в узких терапевтических нишах», отмечается в Стратегии развития фармацевтической промышленности РФ на период до 2030 года, подготовленной Министерством промышленности и торговли РФ.
Например, при поддержке того же Минпромторга под Ростовом Великим создается «Фармославль» — научно-производственный комплекс по разработке и выпуску активных фармацевтических субстанций, которые ранее на территории России не изготавливались. По словам Анастасии Батрак, вице-президента по стратегическому маркетингу группы компаний «Р-Фарм», которая реализует проект, расчетная мощность завода в первый год после запуска превысит 30 тонн субстанций, и компания намерена получить одобрение площадки международными инспекторатами FDA (Food and Drug Administration, США) и ЕМА (European Medicines Agency), что откроет продукции дорогу на зарубежные рынки.
В целом за десять лет российская фармацевтическая промышленность может похвалиться разработкой новых молекул для терапии таких заболеваний, как ВИЧ, гепатит С и сахарный диабет. При государственной поддержке были зарегистрированы 70 конкурентоспособных лекарственных препаратов, некоторые из которых проходят сейчас регистрацию более чем в 60 странах мира.
Вместе с тем, процесс создания новых препаратов настолько трудоемкий с точки зрения финансовых, технологических и научных ресурсов, что политика изоляционизма в этой сфере по меньшей мере неэффективна. Государство хорошо понимает это и не отказывается от сотрудничества с зарубежными компаниями. Напротив, по сути, оно хочет, чтобы Россия стала страной, куда стремятся прорывные инновации со всего мира. Фармкомпании и ведущие исследовательские институты готовы откликнуться на этот призыв — при условии, что заниматься инновациями в России будет комфортно.
«Задача государства заключается в формировании регуляторных условий, премирующих инновационную деятельность, — отмечает генеральный директор „Такеда Россия“, глава региона ICMEA Андрей Потапов. — Необходим комплексный пакет преференциальных мер, которые были бы достаточно гибкими, чтобы адаптироваться к отраслевым изменениям. Я имею в виду нарастающую скорость внедрения инновационных решений, их мультидисциплинарную природу и высокую степень персонализации к течению заболевания пациента».
Система преференций
Если в стратегии «Фарма-2020» меры государственной поддержки в основном стимулировали зарубежных производителей открывать производства на территории России, то сейчас в отношениях власти и бизнеса намечается новый этап развития: важно создать благоприятные условия для проведения в стране ранних клинических исследований.
Что это за условия? Ускоренный процесс регистрации препаратов на территории Российской Федерации, преференциальный доступ к программам бесплатной медицинской помощи, а также премирование при определении цен, полагают участники рынка.
Важна именно система преференций, а не прямая поддержка деньгами, уверен директор Центра оценки технологий в здравоохранении РАНХиГС Виталий Омельяновский: «Уже сейчас мировые производители готовы к переговорам с государством по поводу ценовой политики. Они готовы снижать цену для госзакупок — конечно, при условии, что такая цена не выйдет на международный рынок».
По его словам, в России нужно создавать венчурные фонды, которые будут вкладываться разработку новых молекул и субстанций, а государство станет конечным покупателем уже на той стадии, когда будет доказана их эффективность. «Если говорить об определении инновационного лекарственного препарата, то нужно иметь в виду, что государству важна клиническая эффективность препарата — те параметры, которые ценны для больного и системы здравоохранения. Насколько он, к примеру, уменьшает смертность от заболевания или продлевает жизнь, — рассуждает эксперт. — Революционность препарата должна проявляться именно в этом, а не в особенностях производства и механизме действия».
И здесь российским властям и бизнес-сообществу есть над чем поработать.
Критерии инновационности
«Большинство продуктов, которые позиционируются в России как инновационные, таковыми не являются. Это либо дженерики, либо биоаналоги, либо слегка модифицированные молекулы продуктов, уже существующих на рынке», — отмечалось в исследовании «Разработка инновационных лекарственных препаратов в России: возможности, барьеры и практики», которое в 2014–2015 годах совместно проводили Университет Маастрихта (Maastricht University, Нидерланды) и Национальный исследовательский Томский госуниверситет. За прошедшие годы ситуация, безусловно, улучшилась, но четких критериев и законодательно закрепленного понятия «инновационного препарата» в России до сих пор нет. Пользуясь этим, фармпроизводители могут называть таковым любой новый продукт. Как, в таком случае, государство определит, кто достоин поддержки, а кто нет?
Чтобы создать современную и адекватную запросам времени систему поддержки и оценки инновационных лекарств, стоит использовать опыт стран-участниц клуба 80+. Это, например, Япония, Швеция, Франция, Италия. «В этих странах уделяют очень пристальное внимание оценке инноваций в медицине для того, чтобы включить в программу бесплатной медицинской помощи самые продвинутые и эффективные технологии. Такой подход помогает ранжировать инновации по уровню влияния на систему здравоохранения, а также способствует более рациональным бюджетным затратам», — считает Андрей Потапов из «Такеда Россия».
Например, с 2000 по 2016 год французские власти оценили инновационность 247 лекарственных препаратов, разделив их на пять групп. Если препараты из первой группы оказывают значительный эффект на течение заболевания, то из пятой включаются в программы бесплатной медицинской помощи только при условии экономии средств в сравнении с препаратом-компаратором. В итоге в первую группу вошли только семь препаратов, а 122 не показали достаточный уровень новизны.
«Критерии эффективности инновационных лекарств на государственном уровне есть во многих странах, и рано или поздно они должны появиться и в России, — уверен Виталий Омельяновский. — Дальше — дело за бизнесом».
В итоге выиграют все: местные предприятия станут выпускать больше инновационной продукции, медицинские учреждения опробуют совершенные протоколы лечения, а пациенты получат более качественную медицинскую помощь. Тем самым, Россия сможет поставлять на экспорт не только лекарства, но и медицинские услуги — в виде медицинского туризма.
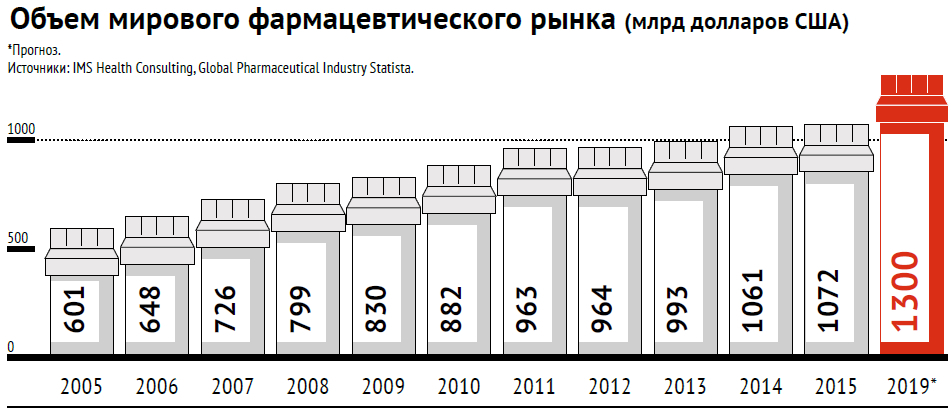
Источник: Официальный журнал Российского инвестиционного форума





































Фонд Росконгресс – социально ориентированный нефинансовый институт развития, крупнейший организатор общероссийских, международных, конгрессных, выставочных, деловых, общественных, молодежных, спортивных мероприятий и событий в области культуры, создан в соответствии с решением Президента Российской Федерации.
Фонд учрежден в 2007 году с целью содействия развитию экономического потенциала, продвижения национальных интересов и укрепления имиджа России. Фонд всесторонне изучает, анализирует, формирует и освещает вопросы российской и глобальной экономической повестки. Обеспечивает администрирование и содействует продвижению бизнес-проектов и привлечению инвестиций, способствует развитию социального предпринимательства и благотворительных проектов.
Мероприятия Фонда собирают участников из 208 стран и территорий, более 15 тысяч представителей СМИ ежегодно работают на площадках Росконгресса, в аналитическую и экспертную работу вовлечены более 5000 экспертов в России и за рубежом.
Фонд взаимодействует со структурами ООН и другими международными организациями. Развивает многоформатное сотрудничество со 197 внешнеэкономическими партнерами, объединениями промышленников и предпринимателей, финансовыми, торговыми и бизнес-ассоциациями в 83 странах мира, с 286 российскими общественными организациями, федеральными и региональными органами исполнительной и законодательной власти Российской Федерации.
Официальные телеграм-каналы Фонда Росконгресс: на русском языке – t.me/Roscongress, на английском языке – t.me/RoscongressDirect, на испанском языке – t.me/RoscongressEsp, на арабском языке – t.me/RosCongressArabic. Официальный сайт и Информационно-аналитическая система Фонда Росконгресс: roscongress.org.